La posologie de Januvia est de 100 mg une fois par jour. En association à la sitagliptine, la posologie
de la metformine et/ou de l'agoniste des récepteurs PPARγ doit être
maintenue.
Quand Januvia est utilisé en association à un sulfamide hypoglycémiant, une réduction de la posologie du sulfamide hypoglycémiant peut être envisagée pour diminuer le risque d'hypoglycémie
(voir rubrique Mises en garde et précautions d'emploi).
En cas d'oubli d'une dose de Januvia, le patient doit prendre cette dose dès qu'il s'en rend compte. Il ne faut pas prendre une double dose le même jour.
Januvia peut être pris au cours ou en dehors des repas.
Patients insuffisants rénaux
Chez les patients présentant une insuffisance rénale légère (clairance de la créatinine [ClCr]
≥ 50 ml/min), aucune adaptation posologique de
Januvia n'est nécessaire.
Chez les patients présentant une insuffisance rénale modérée ou sévère, l'expérience au cours des études cliniques avec Januvia est limitée. L'utilisation de Januvia n'est donc pas
recommandée dans cette population (voir rubrique Propriétés pharmacocinétiques).
Patients insuffisants hépatiques
Chez les patients présentant une insuffisance hépatique légère à modérée, aucune adaptation posologique
n'est nécessaire. Januvia n'a pas été étudié chez les patients ayant une insuffisance hépatique sévère.
Sujets âgés
Aucune adaptation posologique n'est nécessaire en fonction de l'âge. On dispose de données limitées de
tolérance chez les patients âgés ≥ 75 ans. La prudence est donc requise.
Enfants
Compte tenu de l'absence de données d'efficacité et de tolérance, Januvia n'est pas recommandé chez
l'enfant de moins de 18 ans.
Classe pharmacothérapeutique : Inhibiteur de la DPP-4, code ATC : A10BH01.
Januvia appartient à une classe d'hypoglycémiants oraux appelés inhibiteurs de la dipeptidylpeptidase-4
(DPP-4). L'amélioration du contrôle glycémique observée avec ce produit pourrait s'expliquer par l'augmentation des taux des hormones incrétines actives. Les hormones incrétines, notamment le
glucagon-like peptide-1 (GLP-1) et le glucose-dependent insulinotropic polypeptide (GIP), sont libérées par l'intestin tout au long de la journée et leurs taux augmentent en réponse à un
repas. Les incrétines font partie d'un système endogène impliqué dans la régulation physiologique de l'homéostasie du glucose. Lorsque la glycémie est normale ou élevée, le GLP-1 et le GIP
augmentent la synthèse et la libération d'insuline par les cellules bêta du pancréas par des voies de signalisation intracellulaire faisant intervenir l'AMP cyclique. Un traitement par le
GLP-1 ou par des inhibiteurs de la DPP-4 dans des modèles animaux de diabète de type 2 a amélioré la sensibilité des cellules bêta au glucose et stimulé la biosynthèse et la libération
d'insuline. L'augmentation des taux d'insuline entraîne une augmentation de la captation tissulaire du glucose. De plus, le GLP-1 diminue la sécrétion de glucagon par les cellules alpha du
pancréas. La diminution des taux de glucagon associée à l'augmentation des taux d'insuline a entraîné une réduction de la production hépatique de glucose, avec pour conséquence une diminution
de la glycémie. Les effets du GLP-1 et du GIP sont glucose-dépendants de sorte que lorsque la glycémie est basse, il n'y a pas de stimulation de la libération d'insuline et de suppression de
la sécrétion de glucagon par le GLP-1. Pour le GLP-1 et le GIP, la stimulation de la libération d'insuline est accrue lorsque le glucose augmente au-delà des concentrations normales. De plus,
le GLP-1 n'altère pas la réponse normale du glucagon à l'hypoglycémie. L'activité du GLP-1 et du GIP est limitée par l'enzyme DPP-4, qui hydrolyse rapidement les hormones incrétines en
produits inactifs. La sitagliptine empêche l'hydrolyse des hormones incrétines par la DPP-4, d'où une augmentation des concentrations plasmatiques des formes actives du GLP-1 et du GIP. En
augmentant les taux d'incrétines actives, la sitagliptine augmente la libération d'insuline et diminue les taux de glucagon d'une manière glucose-dépendante. Chez les patients diabétiques de
type 2 avec hyperglycémie, ces modifications des taux d'insuline et de glucagon conduisent à une diminution du taux d'hémoglobine A1c (HbA1c) et une diminution des
glycémies à jeun et postprandiale. Le mécanisme d'action glucose-dépendant de la sitagliptine se distingue de celui des sulfamides hypoglycémiants qui augmentent la sécrétion d'insuline même
lorsque la glycémie est basse et qui peuvent entraîner une hypoglycémie chez les patients diabétiques de type 2 et chez les sujets normaux. La sitagliptine est un inhibiteur puissant et
hautement sélectif de l'enzyme DPP-4 et n'inhibe pas les enzymes étroitement apparentées DPP-8 ou DPP-9 aux concentrations thérapeutiques.
Dans une étude de 2 jours réalisée chez des sujets sains, la sitagliptine seule a augmenté la
concentration de la forme active du GLP-1 alors que la metformine seule a augmenté à la fois la concentration totale du GLP-1 et la concentration de sa forme active dans des proportions
similaires. L'administration simultanée de sitagliptine et de metformine a eu un effet additif sur les concentrations de la forme active du GLP-1. La sitagliptine augmente la concentration de
la forme active du GIP, mais pas la metformine.
En résumé de ce qui suit, la sitagliptine administrée en monothérapie, utilisée en association à la
metformine (traitement initial ou ajout), en association à un sulfamide hypoglycémiant (avec ou sans metformine), en association à une thiazolidinedione et en association à une
thiazolidinedione et à la metformine, a amélioré le contrôle de la glycémie, mesuré par des réductions cliniquement significatives du taux d'HbA1c en fin d'étude par rapport aux
valeurs initiales (voir tableau 2).
Deux études ont été réalisées afin d'évaluer l'efficacité et la tolérance de Januvia en monothérapie. Le
traitement par 100 mg de sitagliptine, une fois par jour, en monothérapie, a entraîné des améliorations significatives du taux d'HbA1c, de la glycémie à jeun et de la glycémie
postprandiale à 2 heures versus placebo dans deux études de 18 semaines et 24 semaines. Une amélioration des marqueurs intermédiaires de la fonction des cellules bêta, notamment
l'indice HOMA-β (Homeostasis Model Assessment-β), le rapport proinsuline/insuline et les mesures de la sensibilité des cellules bêta par le test de tolérance glucidique avec prélèvements
répétés a été observée. Chez les patients traités par Januvia, l'incidence des hypoglycémies observées était similaire à celle observée sous placebo. Dans aucune des études, le poids corporel
n'a augmenté par rapport au poids initial au cours du traitement par la sitagliptine comparé à une petite réduction chez les patients ayant reçu le placebo.
Chez des patients présentant un diabète de type 2 et une insuffisance rénale chronique (clairance de la
créatinine < 50 ml/min), une étude a montré que la sécurité d'emploi et la tolérance de doses réduites de sitagliptine étaient généralement similaires à celles du placebo. De plus, les
diminutions des taux d'HbA1c et de la glycémie à jeun observées avec la sitagliptine versus placebo étaient généralement similaires à celles observées dans d'autres études
en monothérapie chez des patients ayant une fonction rénale normale (voir rubrique Propriétés pharmacocinétiques). Le nombre de patients ayant une insuffisance rénale modérée à
sévère était trop faible pour confirmer la sécurité d'emploi de la sitagliptine dans cette population de patients.
Dans deux études de 24 semaines réalisées avec la sitagliptine en ajout soit à la metformine dans l'une,
soit à la pioglitazone dans l'autre, l'ajout de 100 mg de sitagliptine, une fois par jour, a permis d'améliorer significativement les paramètres glycémiques par rapport au placebo. La
modification de poids par rapport à la valeur initiale était similaire chez les patients traités par la sitagliptine et chez ceux recevant le placebo. Dans ces études, l'incidence des
hypoglycémies rapportées était similaire chez les patients traités par la sitagliptine ou le placebo.
Une étude de 24 semaines versus placebo a été réalisée afin d'évaluer l'efficacité et la
sécurité d'emploi de la sitagliptine (100 mg une fois par jour) ajoutée au glimépiride seul ou au glimépiride associé à la metformine. L'ajout de la sitagliptine, soit au glimépiride seul,
soit à l'association glimépiride/metformine, a entraîné des améliorations significatives des paramètres glycémiques. Le poids corporel a légèrement augmenté chez les patients traités par
sitagliptine par rapport à ceux sous placebo.
Une étude de 54 semaines versus placebo a été réalisée afin d'évaluer l'efficacité et la
sécurité d'emploi de la sitagliptine (100 mg une fois par jour) ajoutée à l'association rosiglitazone et metformine. L'ajout de la sitagliptine à l'association rosiglitazone et metformine a
entraîné une amélioration significative des paramètres glycémiques à la semaine 18 (temps de l'analyse principale), avec un maintien de ces améliorations jusqu'à la fin de l'étude. La
modification du poids par rapport au poids initial a été similaire chez les patients traités par la sitagliptine et ceux recevant le placebo (1,9 kg versus 1,3 kg).
Dans une étude factorielle de 24 semaines versus placebo, la sitagliptine 50 mg deux fois par
jour en association à la metformine (500 mg ou 1000 mg deux fois par jour), en traitement initial, a amélioré significativement les paramètres glycémiques par rapport à chacun des traitements
en monothérapie. La réduction du poids avec l'association sitagliptine/metformine était similaire à celle observée avec la metformine seule ou le placebo ; aucune modification du poids par
rapport aux valeurs initiales n'a été observée chez les patients traités par la sitagliptine seule. L'incidence des hypoglycémies était similaire entre les groupes de traitement.
Tableau 2 : Taux d'HbA1c dans les études versus placebo en monothérapie et en
association*
Voir la suite sur : http://www.doctissimo.fr/medicament-JANUVIA.htm




















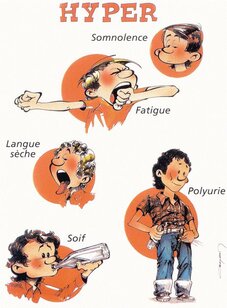









































 Éduquer un diabétique, c’est aussi éduquer son entourage à dépister les signes d’alarme d’une hypoglycémie (malaise, troubles du comportement, agressivité, refus de manger, nausées…).
Éduquer un diabétique, c’est aussi éduquer son entourage à dépister les signes d’alarme d’une hypoglycémie (malaise, troubles du comportement, agressivité, refus de manger, nausées…).



























 2,99 €
2,99 €








































 www.afd.asso.fr/
www.afd.asso.fr/












































 ICI
ICI


