Comprendre l'atrophie musculaire pour mieux la traiter
Aujourd'hui, la plupart des traitements dont on dispose pour accroître la masse musculaire présentent des risques secondaires de développement tumoral. Au-delà de leur usage prohibé dans le milieu sportif, ces substances dites anabolisantes sont
prescrites en cas de perte musculaire inhérente à de nombreuses pathologies graves telles que le diabète, le cancer ou le sida. Mettre au point des thérapies dénuées d'effets secondaires représente donc un réel enjeu.
Les travaux de l'équipe Avenir-Inserm dirigée par Mario Pende et Athanassia Sotiropoulos dévoilent une partie du mécanisme de régulation de la croissance musculaire et
permettent d'ouvrir de nouvelles perspectives dans l'amélioration des thérapies actuelles. Les résultats de cette étude sont détaillés dans l'édition de mars de Nature Cell
Biology.
La perte de masse musculaire est une des conséquences de l'inactivité prolongée et du vieillissement mais aussi de nombreuses pathologies telles que le sida, le diabète ou
le cancer. Pour pallier cette atrophie, divers facteurs
anabolisants (hormones de croissance, IGF1 (insulin-like growth factor),
stéroïdes…) qui agissent sur le volume des muscles peuvent être
prescrits. Malheureusement la plupart de ces thérapies ne sont pas sélectives et induisent à la fois une augmentation du volume et du nombre des cellules
musculaires. Avec un risque majeur : une prolifération anarchique des cellules susceptible d'engendrer des tumeurs.
C'est pourquoi Mario Pende et ses collègues ont étudié les mécanismes de cette croissance musculaire au niveau cellulaire. L'équipe s'est attachée notamment à déterminer si l'augmentation du
volume des cellules musculaires et leur multiplication étaient des processus imbriqués ou indépendants l'un de l'autre.
Deux voies bien distinctes
On sait aujourd'hui que les modifications de la masse musculaire font intervenir la protéine kinase mTOR (mammalian target of rapamycine) : l'exercice physique ou un régime protéique s'accompagnent
d'une activation de mTOR et d'une augmentation de la masse musculaire tandis que l'inactivité, la privation de nourriture ou une thérapie à base de glucocorticoïdes inhibent mTOR et provoquent
une atrophie musculaire.
L'équipe s'est donc penchée sur les mécanismes d'action de mTOR et notamment l'activation de l'un de ses substrats dont le rôle précis restait méconnu : la protéine S6K1(S6 kinase1). Il s'agissait de
comprendre d'une part comment cette protéine pouvait agir sur le volume des cellules et déterminer d'autre part si son activation était à la fois impliquée dans la multiplication et dans la
croissance des cellules musculaires.
A l'issue de ces recherches, Mario Pende et ses collègues ont mis en évidence le rôle essentiel joué par cette protéine S6K1 dans un mécanisme qui coordonne la croissance
des différents tissus musculaires en fonction des nutriments
apportés. On savait que dans le cas d'un régime protéique, les acides
aminés des protéines agissent directement sur les muscles et libèrent parallèlement des substances anabolisantes dans le sang. L'équipe a démontré que le
gène S6K1 intégrait tous ces signaux pour produire de nouvelles protéines qui
augmentent la masse musculaire. En fait, c'est en inhibant ce gène que les chercheurs ont pu démontrer son rôle. « Nous avons montré que les animaux chez lesquels le gène S6K1 a été
invalidé restent maigres, même s'ils sont nourris avec un régime riche en protéines qui devrait normalement accroître leur masse musculaire » précise Mario Pende. L'inhibition de S6K1 suffit donc à produire une atrophie musculaire et une perte de poids.
Dans un deuxième temps, l'équipe a montré que l'inhibition du gène S6K1 n'avait aucun effet sur la prolifération cellulaire : les cellules musculaires sont plus
petites mais leur nombre reste normal. « En clair, nous avons prouvé que le contrôle du cycle cellulaire musculaire par mTOR ne passait pas par S6K1 » Les chercheurs concluent qu'il
existe bien deux branches distinctes et indépendantes dans la voie mTOR, dont l'une nécessite l'activation de S6K1 et agit uniquement sur le volume des cellules. L'autre voie qui contrôle la
prolifération reste donc à explorer.
Etant donné que S6K1 est indispensable à l'augmentation de la taille des cellules mais n'a pas d'action sur la prolifération, ces travaux sur la souris ouvrent des
perspectives dans la recherche de nouvelles thérapies. On peut notamment envisager d'ici une dizaine d'années de mettre au point des traitements de l'atrophie
musculaire basés sur l'activation de S6K1 et qui présenteraient un faible risque de tumeurs.
http://www.futura-sciences.com/fr/news/t/vie-1/d/comprendre-latrophie-musculaire-pour-mieux-la-traiter_5868/




















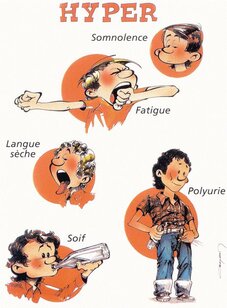










































 Éduquer un diabétique, c’est aussi éduquer son entourage à dépister les signes d’alarme d’une hypoglycémie (malaise, troubles du comportement, agressivité, refus de manger, nausées…).
Éduquer un diabétique, c’est aussi éduquer son entourage à dépister les signes d’alarme d’une hypoglycémie (malaise, troubles du comportement, agressivité, refus de manger, nausées…).



























 2,99 €
2,99 €








































 www.afd.asso.fr/
www.afd.asso.fr/












































 ICI
ICI


