Maladie de Parkinson : les chercheurs sur de nouvelles pistes
Par Janlou Chaput, Futura-Sciences
La maladie de Parkinson, ou plutôt les maladies de
Parkinson, comme l’explique à Futura-Sciences le neurologue Pierre Cesaro, restent encore mal connues. Plusieurs pistes sont aujourd'hui explorées, notamment le traitement personnalisé grâce à la
génomique. Ces avancées prometteuses laissent espérer des progrès majeurs
dans les années à venir.
Après Alzheimer, la maladie de Parkinson est la deuxième affection neurodégénérative pour l’incidence mondiale. La recherche s’implique beaucoup pour tenter d'en comprendre les causes, multiples, et proposer des thérapies pour chaque patient.
Alors on teste de nombreux traitements, on explore un maximum de pistes, on fait muter des
mouches drosophiles pour qu’elles déclarent les symptômes… Tout cela finira bien par mener les scientifiques sur la bonne voie, tôt ou tard. Les
dernières recherches montrent d’ailleurs que les mutants dits parkin peuvent être un modèle (parmi d’autres) pour étudier la maladie.
Des travaux publiés en janvier dans Human Molecular Genetics révèlent que ces insectes malades connaissent des défaillances métaboliques liées à des problèmes intrinsèques aux
mitochondries. En découle alors une accumulation cellulaire de
lactate, que les chercheurs proposent d’utiliser comme biomarqueur afin
d’établir un diagnostic précoce de la forme de la maladie qui touche les individus les plus jeunes.
Anticiper pour mieux traiter la maladie de Parkinson
Pierre Cesaro, chef du service de neurologie à l’hôpital Henri-Mondor de Créteil (94), confirme à
Futura-Sciences l’intérêt de telles études. « On recherche en effet des biomarqueurs pour un diagnostic plus précoce, car on sait que la quasi-totalité des patients commencent à développer la
maladie bien avant la manifestation des symptômes classiques. » Gagner du temps permettra de ralentir la progression de la neurodégénérescence. « Une étude portant sur une molécule, la rasagiline, montre qu’elle retarde de 30 % l’aggravation des symptômes,
après le début de ceux-ci. »
Aujourd’hui, nous en avons les moyens techniques, grâce à l’imagerie scintigraphique au DAT scan, capable d’anticiper la maladie de plusieurs années. « Mais l’examen est très coûteux et
il est impossible de l’utiliser à grande échelle. D’où la nécessité de trouver un biomarqueur, comme le lactate. S’il fait ses preuves, ce qui reste encore à démontrer. »


Le docteur Pierre Cesaro est le chef du service de neurologie à l'hôpital Henri-Mondor à Créteil. Il est l'un des spécialistes français de la maladie de Parkinson. © DR
Appelons-les plutôt les maladies de Parkinson
Mais voilà, la maladie est multifactorielle, et les symptômes peuvent varier d’un patient à l’autre. À tel point qu’il paraît plus juste de parler des maladies de Parkinson. Ce qui complique
d’autant plus la tâche des scientifiques !
Si l’on sait que la génétique explique à elle seule 5 % des cas
(principalement chez les individus jeunes) et que 30 % des patients sont dotés de prédispositions génétiques (si l’on se limite
aux gènes connus…), l’environnement aurait lui aussi son rôle à jouer, à
travers les pesticides organochlorés ou certains métaux, parmi les coupables identifiés… Mais beaucoup courent encore dans la nature et n’ont pas été
rattrapés par les chercheurs.
Inéluctablement, chaque cas doit se traiter individuellement en fonction des symptômes qui se manifestent. « Un nouveau domaine prometteur est en plein essor : la pharmacogénomique,
poursuit Pierre Cesaro pour Futura-sciences. Cette discipline vise à étudier l’interaction entre le génome et un médicament absorbé pour, à terme, personnaliser les traitements. »
De la DOPA…
À l’heure actuelle, les thérapies portent quasi exclusivement sur des médicaments à base de DOPA, une molécule qui, une fois métabolisée, se transforme en dopamine, un neurotransmetteur fondamental qui se trouve en situation déficitaire dans certaines régions
cérébrales. Les anticholinergiques constituent l’autre forme de
traitement médicamenteux, car on connaît depuis plusieurs décennies leur efficacité contre le tremblement, une caractéristique bien connue des maladies de Parkinson.
Mais il n’y a pas que la biochimie pour corriger les troubles. La stimulation cérébrale profonde, qui consiste à implanter des électrodes à même le cerveau, a fait ses preuves. En France, 3.500 personnes ont eu recours à cette
thérapie, qui se pratique désormais chaque année sur 200 à 350 personnes.


Les rayons X permettent de visualiser les électrodes utilisées en cas de
stimulation cérébrale profonde. Dans ce cas de figure, les implants apparaissent au sommet du crâne au départ desquels les câbles sont reliés. En revanche, les tâches blanches au niveau de la
mâchoire n'ont aucun rapport (ce sont des dents en métal). © Hellerhoff, Wikipédia, cc by sa 3.0
… À la stimulation cérébrale profonde
Une étude parue dans The Lancet Neurology ces dernières semaines vient encore de le démontrer. Des
patients atteints par la maladie depuis cinq ans minimum et présentant des dyskinésies (les mouvements anormaux et les tremblements) au moins six heures par jour ont subi l’opération
chirurgicale en recevant les électrodes au niveau des noyaux subthalamiques. Les bénéfices sont bien réels. La qualité de vie des 168 sujets en a été grandement améliorée : en moyenne 4 heures 15
de temps de répit supplémentaire chaque jour.
« Depuis 1993 et la première expérience, on connaît son efficacité. Seulement il y a de nombreux effets secondaires, explique Pierre Cesaro.
Saignements, infections bactériennes peuvent compliquer la chirurgie,
qui peut aussi induire des effets psychiques importants, comme des confusions, des troubles de la parole, et 30 % des personnes traitées deviennent apathiques. Ce traitement ne résout pas tous
les problèmes moteur et ne peut pas être proposé aux personnes de plus de 70 ans, qui représentent pourtant la grande majorité des malades. »
D’autres régions sont alors ciblées pour tenter de mettre au point un traitement sans contrindication, utilisable de 7 à 77 ans. Parmi elles : le cortex moteur, le noyau pédonculopontin, le pallidum ou la moelle épinière.
La pharmacopée du futur
La thérapie contre Parkinson se résume à cela actuellement. Mais de nouveaux traitements sont en cours d’essais cliniques. « Au mieux, ils sont en phase III, et à ma connaissance aucun n’est
commercialisé » nous confie le neurologue.
Parmi les cibles de ces médicaments,
le glutamate, un acide aminé qui sous cette forme devient le neurotransmetteur excitateur le plus important du système
nerveux et qui est à l’origine de complications motrices involontaires. L’adénosine, molécule impliquée dans le système de médiation du cerveau, se trouve également dans la ligne de mire des principes actifs de demain. Tout comme les
récepteurs cannabinoïdes.
Petit à petit, les traitements se diversifient, et devront probablement s’additionner pour bloquer tous les différents symptômes. Mais soigner les manifestations du mal ne revient pas à soigner le mal
lui-même. Bloquer la neurodégénérescence dans l’œuf reste l’étape ultime à atteindre. Il faudra encore du temps avant qu’on y parvienne. Mais la recherche progresse à grands pas !
http://www.futura-sciences.com/fr/news/t/medecine/d/maladie-de-parkinson-les-perspectives-a-venir_36743/#xtor=EPR-17-[QUOTIDIENNE]-20120221-[ACTU-maladie_de_parkinson_:_les_chercheurs_sur_de_nouvelles_pistes]




















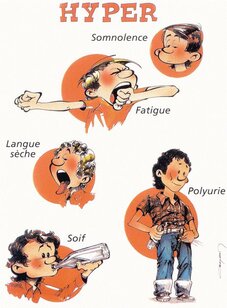









































 Éduquer un diabétique, c’est aussi éduquer son entourage à dépister les signes d’alarme d’une hypoglycémie (malaise, troubles du comportement, agressivité, refus de manger, nausées…).
Éduquer un diabétique, c’est aussi éduquer son entourage à dépister les signes d’alarme d’une hypoglycémie (malaise, troubles du comportement, agressivité, refus de manger, nausées…).



























 2,99 €
2,99 €








































 www.afd.asso.fr/
www.afd.asso.fr/












































 ICI
ICI




